
Hidrolisis Garam Kimia Kelas 11 • Part 5 Contoh Soal Perhitungan pH Larutan Garam (2) YouTube
Oleh karena itu garam dapat terbentuk dari 4 reaksi kimia sebagai berikut: 1. Garam dari asam kuat dan basa kuat, dimana garam ini akan memiliki pH = tujuh alias bersifat netral, yang artinya tidak terjadi hidrolisis. 2. Garam dari asam kuat dan basa lemah, garam akan memiliki pH < tujuh alias bersifat asam. 3.

Hidrolisis Garam dari Asam lemah dan Basa Kuat Rumus Kimia
Tetapan keseteimbangan reaksi hidrolisis disebut tetapan hidrolisis (Kw). pH larutan garam dari asam kuat dan basa kuat yang tepat habis bereaksi adalah pH = 7 (netral).. Rumus, dan Penerapannya Juni 13, 2023. Materi Kimia Gaya Antar Molekul, Jenis dan Penerapannya

Pengertian Larutan Garam, Sifat, Ciri, Jenis dan Contohnya
Tetapan hidrolisis (Kh) dari reaksi hidrolisis tersebut yaitu: Besarnya pH garam ditentukan dari konsentrasi ion OH - dalam larutan garam tersebut, dengan menggunakan rumus sebagai berikut. Keterangan: K a = tetapan kesetimbangan asam. K w = tetapan kesetimbangan = 10-14. K h = tetapan hidrolisis [G] = Konsentrasi anion garam terhidrolisis. 3.

Hidrolisis Garam Pengertian, Macam, Dan Rumus, Beserta Contoh Soalnya Secara Lengkap
Skala pH berkisar dari 0 hingga 14, di mana angka 7 menunjukkan larutan netral, angka di bawah 7 menunjukkan larutan asam, dan angka di atas 7 menunjukkan larutan basa. Hidrolisis Garam. Hidrolisis garam terjadi ketika garam yang dilarutkan dalam air mengalami reaksi dengan air.

Hidrolisis Garam Kimia Kelas 11 • Part 2 Perhitungan pH Larutan Garam Terhidrolisis Parsial
Garam yang terbentuk dari proses netralisasi antara asam kuat dan basa lemah akan bersifat asam. Contohnya NH4Cl, FeCL₃, CuCl₂, AlCl₃, CuSO₄, dan lain-lain. Begini persamaannya: NH 4 Cl (aq) = Cl - (aq) + NH 4+ (aq) Ion amonium yang terbentuk mengalami hidrolisis garam untuk membentuk amonium hidroksida dan ion H⁺.

Garam Berikut Yang Mengalami Hidrolisis Sebagian Adalah Blog Yuri
Hidrolisis Garam: Pengertian, Macam-Macam, dan Jenisnya. Hidrolisis garam - Suatu asam yang bereaksi dengan suatu basa akan menghasilkan senyawa ionik berupa garam. Sementara larutan memiliki beberapa kemungkinan sifat yaitu asam, basa ataupun netral. Hal ini disebabkan adanya hidrolisis pada garam, yakni reaksi dari kation atau anion atau.

Konsep mudah menentukan reaksi hidrolisis garam dan menghitung pH garam. Kimia SMA YouTube
Rumus Hidrolisis Garam. 1. Garam yang terbentuk dari komponen asam lemah dan basa kuat. Garam yang berasal dari asam lemah dan basa kuat dalam air akan mengalami hidrolisis sebagian. Komponen garam (anion asam lemah) mengalami hidrolisis menghasilkan sebuah ion OH -, maka pH > 7 sehingga larutan garam bersifat basa.

Perhatikan tabel persamaan reaksi hidrolisis garam beriku...
Oleh karena itu, larutan garam dari asam lemah dan basa kuat akan meningkatkan konsentrasi OH − dalam air sehingga larutannya bersifat basa (pH > 7).. Garam dari asam lemah dan basa lemah. Garam seperti CH 3 COONH 4 yang dapat terbentuk dari reaksi asam lemah (CH 3 COOH) dan basa lemah (NH 3) akan mengalami hidrolisis kation dan anionnya. pH larutan garam demikian bergantung pada kekuatan.

PH HIDROLIS GARAM (Part 1) YouTube
Untuk lebih memahami mengenai rumus hidrolisis garam, maka perlu untuk mempelajari beberapa contoh soal berikut beserta dengan pembahasannya. 1. Hitunglah pH dari larutan garam NH4CN 0,2 M. Jika, diketahui Ka HCN = 4,0 x 10^-10 mol/L dan Kb NH3 = 1,8 x 10 10^-5 mol/L !

LENGKAP UNTUK PEMULA ‼️ HIDROLISIS GARAM PART2 ‼️ CARA MENULISKAN REAKSI HIDROLISIS YouTube
Kh = konstanta hidrolisis Harga pH garam yang tersusun dari asam lemah dan basa lemah tergantung pada harga Ka dan Kb a. Apabila Ka = Kb maka larutan bersifat netral (pH = 7). Karena KCN bersifat basa, maka rumus yang digunakan untuk mencari pH seperti berikut. Maka, pH = 14 - 2,5 + log 1,75 = 11,75 + log 1,75. 5.

Soal Hidrolisis Garam Dan Penyelesaiannya
Reaksi hidrolisis ini menghasilkan ion H+ atau OH-. Contoh diatas, menjelaskan bahwa kedua komponen penyusun garam CH3COO- (anion dari asam lemah) dan NH4+ (kation dari basa lemah) dapat terhidrolsis secara sempurna yang masing-masing berurutan menghasilkan ion yang bersifat basa (OH-) dan ion yang bersifat asam (H+).

LENGKAP ‼️ CARA MENGHITUNG pH HIDROLISIS GARAM KELAS 11 YouTube
Selain itu, kamu bisa mendapatkan contoh soal hidrolisis garam sebagai latihanmu. 2. pH Larutan hidrolisis. Materi selanjutnya yang akan kamu pelajari adalah materi mengenai menghitung pH larutan hidrolisis. Untuk menghitung pH larutan hidrolisis, kamu harus menentukan terlebih dahulu jenis garam yang akan dihidrolisi.

PPT Rumus pH Hidrolisa PowerPoint Presentation, free download ID4714439
Sifat-Sifat pH Larutan Garam. Rumus pH Larutan Garam. Contoh Soal Hidrolisis Garam. Contoh Soal #1: Contoh Soal #2: Jika makanan terasa hambar, tentunya Sobat Pijar akan menambahkan garam agar rasanya menjadi asin. Salah satu senyawa garam paling umum adalah NaCl atau biasa dikenal dengan garam dapur yang biasa Sobat Pijar konsumsi sehari-hari itu.
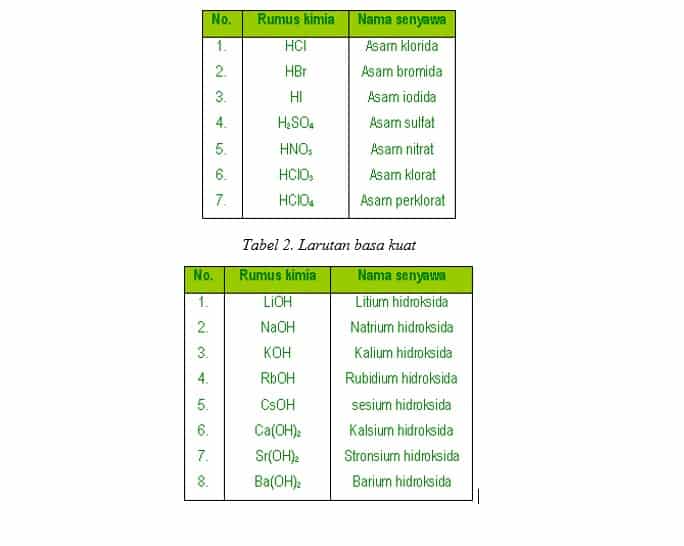
Hidrolisis Garam Pengertian, Macam, Dan Rumus, Beserta Contoh Soalnya Secara Lengkap
Verifying that you are not a robot.

PH hidrolisi garamsoal menentukan massa dari pH kimia SMA YouTube
Sifat asam atau basa larutan yang dihasilkan hidrolisis garam bergantung pada jenis asam basa yang membentuk garam tersebut. Baca juga: Hukum Kekekalan Energi: Pengertian, Rumus, dan Penerapannya. Misalnya garam yang terbentuk dari asam kuat dan basa kuat, garam yang terbentuk dari asam kuat dan basa lemah, garam yang terbentuk dari asam lemah.

Menentukan Kh dan pH hidrolisis Garam KIMIA SMA YouTube
Penurunan Rumus pH Hidrolisis garam asam lemah dan basa kuat. Garam yang berasal dari asam lemah dan basa kuat bersifat basa, contohnya Na CO, CH COOK, dan NaCN. Pada garam ini yang mengalami hidrolisis adalah anionnya (A) dengan reaksi:b. sehingga: pH = 14 - pOH .