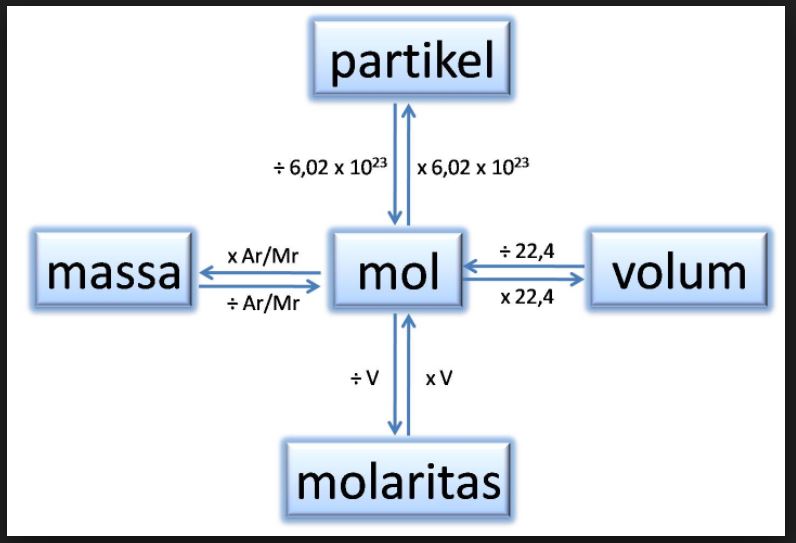
Hubungan Mol dengan Jumlah Partikel dan Massa Zat Read HSTKB
Rumus Perhitungan Molalitas dan Contoh Soal Jawab. Perhitungan Molalitas - Materi Kimia berikut tentang Perhitungan Molalitas . Dalam perhitungan molaritas, kuantitas larutan didasarkan pada volume. Sahabat tentu tahu bahwa volume merupakan fungsi suhu (zat akan memuai ketika dipanaskan). Oleh karena sifat koligatif larutan dipengaruhi suhu.

apa perbedaan molalitas dan molaritas Brainly.co.id
Rumus normalitas kimia adalah N = n x a /V, yang menyatakan nilai normal (N) yang sama dengan satu mol ekivalen/liter. Dalam kimia, terdapat beberapa besaran yang dapat digunakan untuk menyatakan suatu konsentrasi zat terlarut dalam sebuah larutan antara lain yaitu molaritas, molalitas, normalitas dan fraksi mol.

Mengenal Rumus Molaritas dan Molalitas Konsentrasi Larutan
Dalam sub pembahasan molalitas dan fraksi mol yang akan dibahas kali ini adalah mengenai pengertian molalitas, hubungan molalitas dengan persen massa, hubungan molalitas dengan molaritas, perbedaan molalitas dan molaritas pengertian fraksi mol, rumus fraksi mol zat pelarut (Xp) dan rumus fraksi mol zat terlarut (Xt). Berikut penjelasannya. 1.
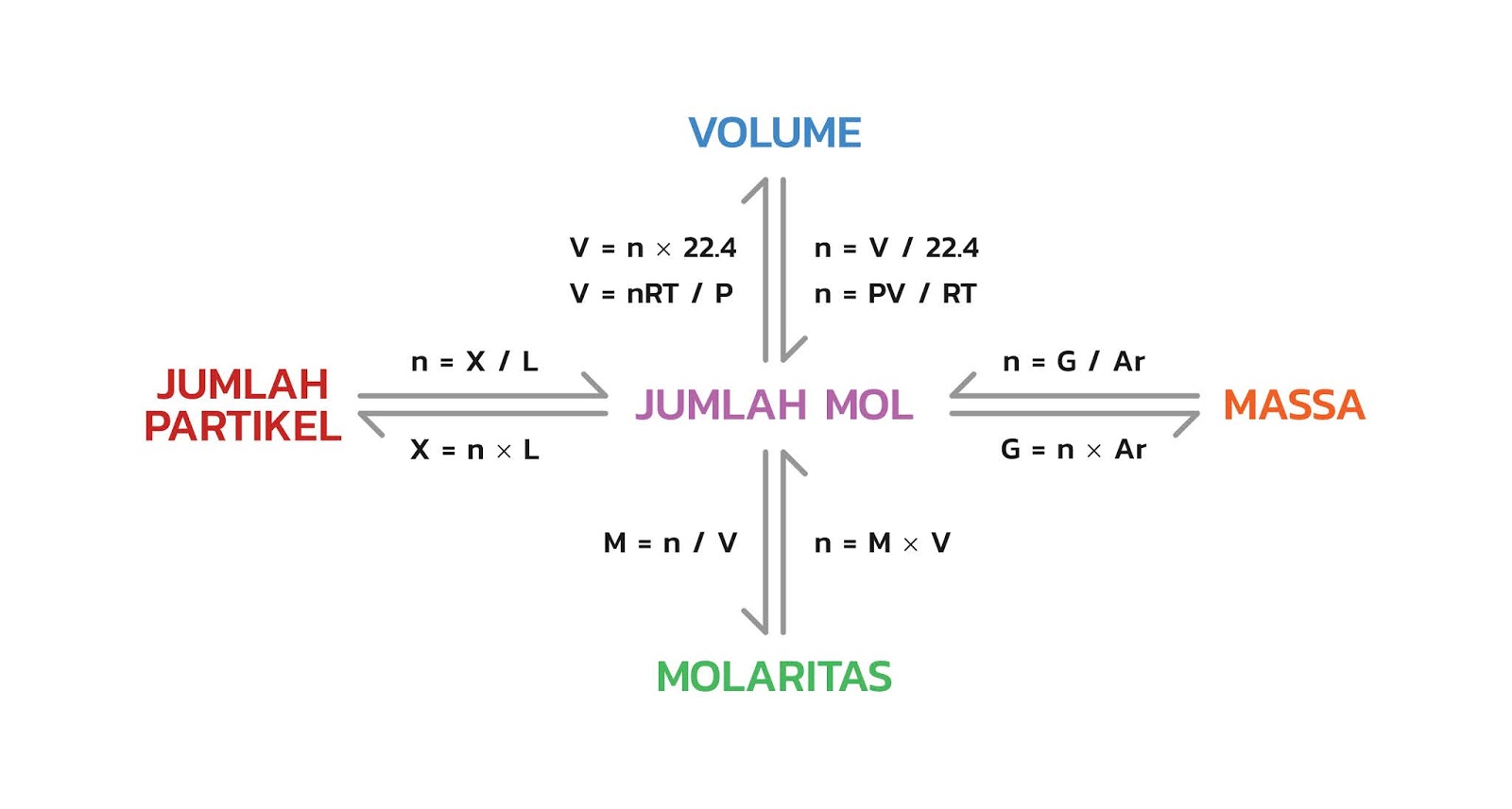
Hubungan Mol Dengan Jumlah Partikel Massa Volume Dan Molaritas Riset
Rumus Molaritas. Molaritas termasuk konsentrasi larutan. Dari berbagai bentuk konsentrasi yang dipengaruhi sifat koligatif larutan yaitu molaritas, molalitas, dan fraksi mol. Satuan molaritas adalah mol/liter atau M. Rumus molaritas yaitu mol zat terlarut dibagi volume larutan. Tetapi, molaritas dapat dicari melalui massa jenis zat terlarut dan volume larutan.

Rumus molaritas molalitas normalitas dan fraksi mol 2021
Misalnya, molalitas suatu larutan adalah 12 mol/kg, maka dapat dinyatakan sebagai 12 molal atau 12 m. Baca juga: Soal UAS Kimia: Prinsip Molalitas dan Molaritas. Rumus molalitas. Seperti yang telah dikatakan sebelumnya, molalitas adalah jumlah mol zat terlarut dalam 1.000 gram pelarut. Maka, rumus molalitas adalah: Dengan,

Rumus Molaritas dan Molalitas
Demikian pembahasan tentang molalitas hingga rumus molalitas beserta soalnya. Semoga setelah membaca artikel ini sampai selesai, Grameds jadi lebih mudah dalam mengerjakan soal molalitas. Untuk mendukung Grameds dalam menambah wawasan, Gramedia selalu menyediakan buku-buku berkualitas dan original agar Grameds memiliki informasi #LebihDenganMembaca

Kimia 12 Molaritas Molalitas dan Fraksi Mol YouTube
Garam tersebut memiliki massa molekul relatif sebesar 58,5 gram/ mol. Hitung mol dari gram! Demikian penjelasan mengenai rumus molaritas dan molaitas, disertai dengan contoh soalnya. Pertarungan politik menuju Pemilu 2024 makin panas. Baca artikel untuk mengungkap kejutan dan kontroversi yang akan terjadi dalam pemilihan nanti!

Rumus Molaritas Normalitas Dan Molalitas PDF
Rumus Molaritas. Molaritas ini merupakan jenis konsentrasi larutan yang dipengaruhi oleh sifat koligatif larutan, yaitu molaritas, molalitas, dan fraksi mol. Rumus molaritas sendiri adalah mol zat terlarut yang dibagi dengan volume larutan, sementara satuannya adalah mol/liter atau M.

Perbedaan Rumus Molaritas Dan Molalitas 52 Riset
Supaya elo makin paham dengan materi rumus molaritas dan molalitas, gue sudah menyediakan contoh soal dan pembahasannya nih. Elo siapkan alat tulisnya juga ya untuk ikut mengerjakan! Contoh Soal 1. Garam dapur (NaCl) memiliki massa 10 gram. Garam tersebut memiliki massa molekul relatif sebesar 58,5 gram/mol. Hitunglah mol dari garam!
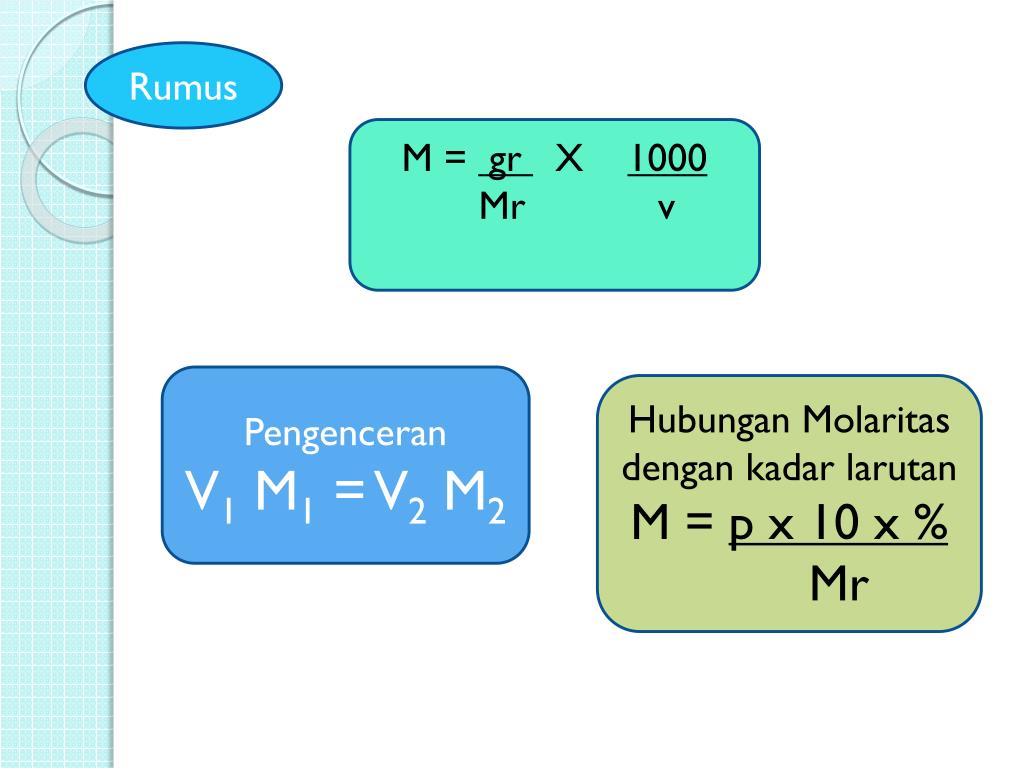
PPT MolaRitas PowerPoint Presentation, free download ID5565192
Perbedaan Molalitas dan Molaritas. Molaritas (M) ailah banyaknya mol zat terlarut dalam 1 liter larutan, sedangkan Molalitas (m) ialah banyaknya mol zat terlarut dalam 1kg pelarut. Moralitas ( M ) yaitu satuan konsentrasi yang banyak dipakai dan didefinisikan sebagai banyak mol zat terlarut dalam 1 liter larutan dalam satuan M. Sedangkan

Rumus Molaritas, Definisi, Persamaan Molaritas, Contoh Soal
Molaritas, molalitas dan normalitas merupakan salah satu satuan dalam konsentrasi larutan yang berguna untuk menyatakan hubungan kuantitatif antara zat terlarut dan zat pelarut. Untuk lebih jelasnya dibawah ini akna dijelaskan tentang pengertian Molaritas, Molalitas dan Normalitas lengkap dengan rumus dan contoh soalnya.
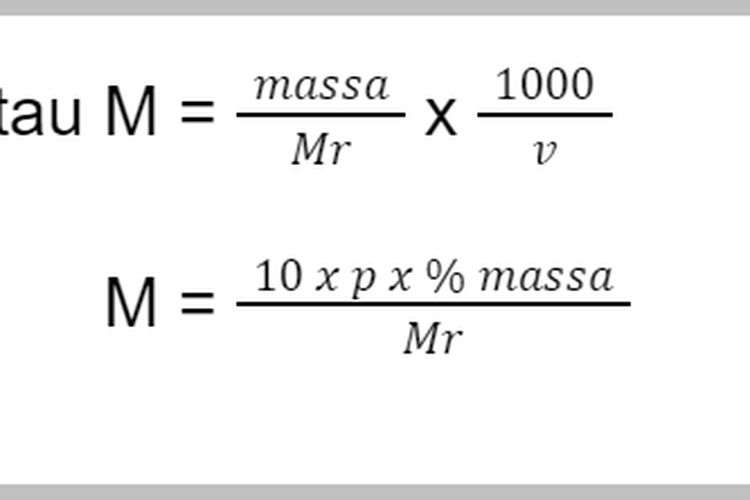
Pahami Rumus Molaritas, Contoh Soal, dan Pembahasannya Berikut Ini
Perbedaan Rumus Molaritas dan Molalitas. Sebelum kita membahas lebih lanjut antara keduanya, kita harus mengetahui secara definisi, apa sih itu molaritas dan molalitas? by definition, Molaritas menyatakan jumlah mol suatu zat per liter. Molaritas ini dilambangkan dengan huruf "M" dengan satuannya molar atau M yang setara dengan mol/liter.

Rumus Molaritas cara membatalkan pesanan
Ketahui rumus dasar dari menghitung molaritas. Molaritas menunjukkan hubungan antara jumlah mol terlarut per liter larutan, atau volume larutan tersebut. Dalam rumus, molaritas dituliskan sebagai: molaritas = mol terlarut / liter larutan. Contoh soal: Berapakah molaritas larutan yang terbentuk dengan melarutkan 3,4 g KMnO 4 dalam 5,2 liter air?

Pengertian Molaritas, Rumus dan Contohnya
Untuk menghitung molaritas, kita dapat menggunakan rumus molaritas. Berikut adalah rumus-rumus molaritas! M = g/Mr x 1.000/V atau M = n/V. Dengan, M: molaritas (mol/L) n: jumlah mol zat g: massa zat terlarut (gram) Mr: massa molekul relatif zat terlarut (g/mol) V: volume larutan (mL) Baca juga: Soal UAS Kimia: Prinsip Molalitas dan Molaritas.

Cara Menghitung Molaritas, Molalitas, dan Fraksi Mol YouTube
Rumus Molaritas dan Molalitas & Contoh Soal. Sifat koligatif larutan merupakan salah satu materi kimia yang ada di kelas XI SMA. Supaya memahami materi ini, kamu wajib menguasai rumus molaritas dan molalitas larutan dengan baik karena bab ini memiliki hubungan yang erat dengan konsentrasi larutan. Bagi kamu yang belum tahu, larutan adalah.

Molalitas Pengertian, Satuan, Rumus, dan Contoh Soal Menghitungnya
Rumus Normalitas, Molaritas, dan Molalitas - Rumus normalitas, molaritas, dan molalitas merupakan pelengkap dari pembahasan mengenai unit maupun satuan untuk menyatakan konsentrasi larutan. Materi ini secara umum dijelaskan melalui mata pelajaran IPA atau Ilmu Pengetahuan Alam pada jenjang pendidikan SMA atau sederajat.